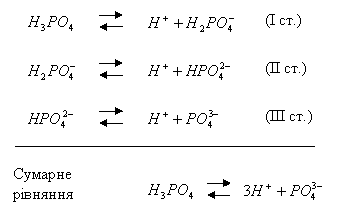
Як дисоціює ортофосфатна кислота?
У водних розчинах ортофосфатна кислота дисоціює ступінчасто:
- H 3 P O 4 ⇄ H + + H 2 P O 4 − ,
- H 2 P O 4 − ⇄ H + + HP O 4 2 − ,
- HP O 4 2 − ⇄ H + + P O 4 3 − .
Як писати рівняння дисоціації?
Ступінь електролітичної дисоціації. Відношення числа дисоційованих часток до вихідного числа часток розчиненої речовини за певної температури називається ступенем дисоціації. Позначення: α (альфа), визначальне рівняння: α = n/N, де n – число дисоційованих часток, N – вихідне число часток розчиненої речовини.
Як дисоциюють кислоти?
Кислоти дисоціюють на катіони Гідрогену й аніони кислотного залишку. Луги дисоціюють на катіони металу (або йони амонію) та аніони гідроксидної групи. Солі дисоціюють на катіони металу (або йони амонію) та аніони кислотного залишку.
Що утворюється при дисоціації кислот?
З точки зору теорії електролітичної дисоціації кислоти — це електроліти, які при дисоціації утворюють катіони Гідрогену.
H3PO4 = H(+) + H2PO4(-). H2PO4(-2) = H(+) + HPO4(-2). HPO4(-2) = H(+) + PO4(-3). H3PO4 = 3H(+) + PO4(-3). Диссоциация процесс обратимый.
3) розрахуйте кількість йонів, яку дає ортофосфатна кислота при повній дисоціації кількістю речовини 1 моль, підтвердіть рівнянням дисоціації і …
середньої сили (ортофосфатна, тощо);. слабкі (карбонатна, сульфідна, тощо). Проаналізуємо рівняння дисоціації сильних кислот. Дисоціація хлоридної кислоти:.